【プレスリリース】人工設計によるαヘリックス型ペプチドナノポアの創出と一分子センシングの実証に成功
概要
横浜国立大学大学院工学研究院機能の創生部門 川村出教授、東京農工大学大学院工学研究院生命機能科学部門の川野竜司教授、同大学院GIR研究院のPeng Zugui特任助教、同大学院工学府大学院生(当時)の宇佐美将誉氏、關谷(せきや)悠介氏、同大学院工学府大学院生(在学中)の中田彩夏氏、藤田祥子氏、モンゴル国立大学のMijiddorj Batsaikhan准教授らからなる研究グループは、人工的に設計したペプチド[用語1]によりαヘリックス[用語2]構造を有するナノポア[用語3]の作製に成功し、そのナノポアを用いた一分子検出を実現しました。本成果は、DNAやタンパク質の高精度解析に役立つバイオセンサーや次世代の医療診断ツールへの応用に加え、人工細胞や分子機械の基盤技術としての発展が期待されます。
背景
近年、ナノポア計測と呼ばれる一分子計測技術が大きな注目を集めています。ナノポアとは、細胞膜に形成される極めて微小な孔であり、分子が通過する際の電流変化を利用して、一分子レベルでの観察を可能にするものです。この技術は、既にDNAシーケンスや分子識別など幅広い応用が進められています。従来は天然タンパク質由来のナノポアが主に利用されてきましたが、その種類は限られており、目的に応じて自由に設計することは困難でした。そこで現在、人工的に新しいナノポアを設計・構築する研究が活発に進められています。しかし、人工細胞膜中で安定に存在し、かつ十分な大きさを持つ孔を人工的に形成することは容易ではなく、長年の課題となっていました。
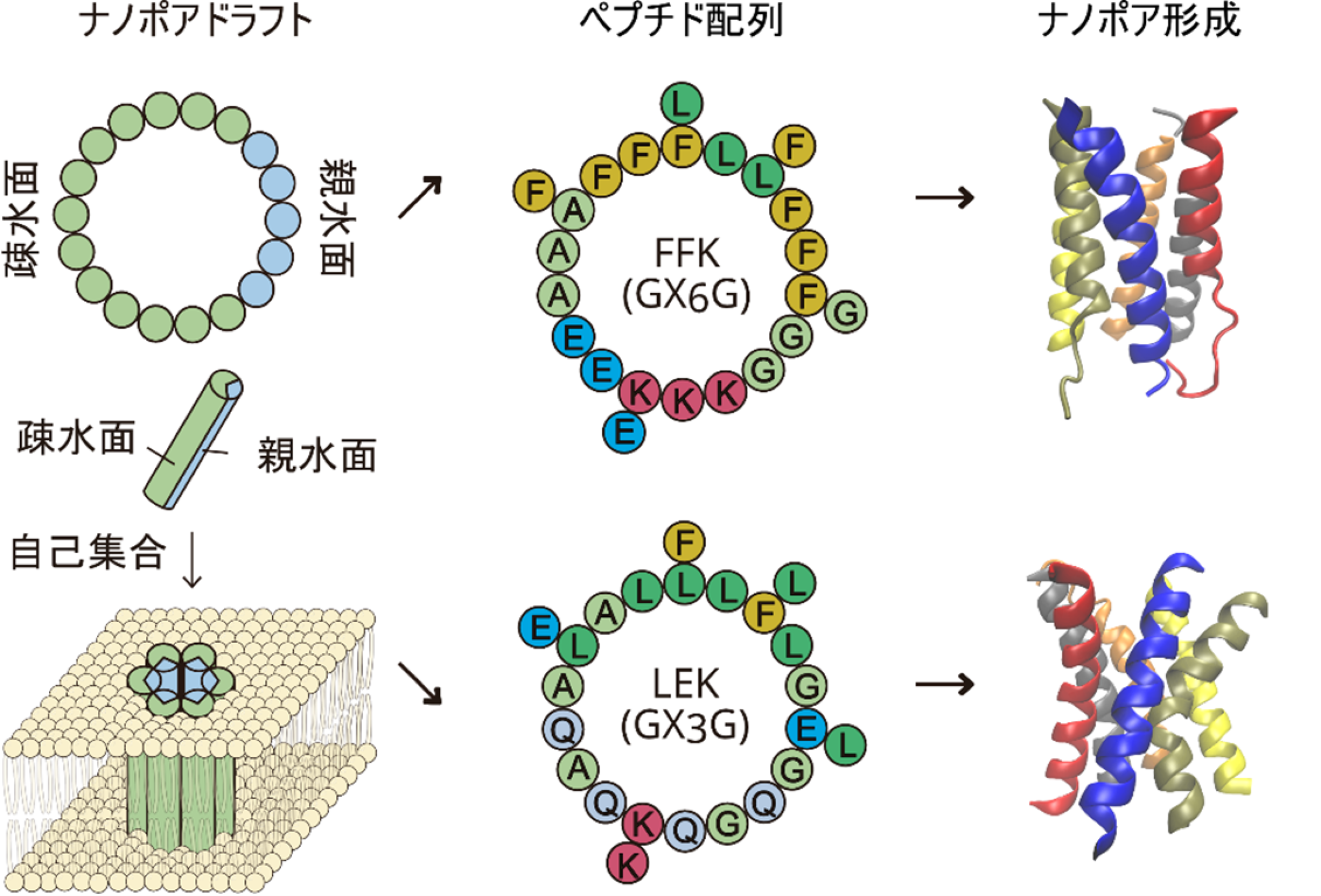
本研究では、この課題に取り組むため、天然タンパク質に多く見られる「GASモチーフ」[用語4]と呼ばれるアミノ酸配列を基盤に、FFKおよびLEKという二種類の人工ペプチドを設計しました。計算機シミュレーションと実験の両面から検証を行い、これらのペプチドが実際に膜中で孔を形成し、イオンや分子が侵入することができることを明らかにしました。
研究体制
本研究は、東京農工大学大学院工学研究院生命機能科学部門の川野竜司教授、同大学院GIR研究院のPeng Zugui特任助教、同大学院工学府大学院生の宇佐美将誉(当時)、關谷悠介(当時)、中田彩夏、藤田祥子、モンゴル国立大学のMijiddorj Batsaikhan准教授、横浜国立大学大学院工学研究院機能の創生部門 川村出教授らによって実施されました。本研究はJSPS学術変革領域研究(A)「De novo細胞膜分子システムのボトムアップ構築」JP21H05229、若手研究「アミノ酸配列解析のためのDNA-ペプチドコンジュゲートナノポアの構築」JP24K17705、科学技術振興機構(JST)戦略的創造推進事事業 CREST「自在配列設計ペプチドによるナノポアシステムの構築」JPMJCR21B2の助成を受けたものです。
研究成果
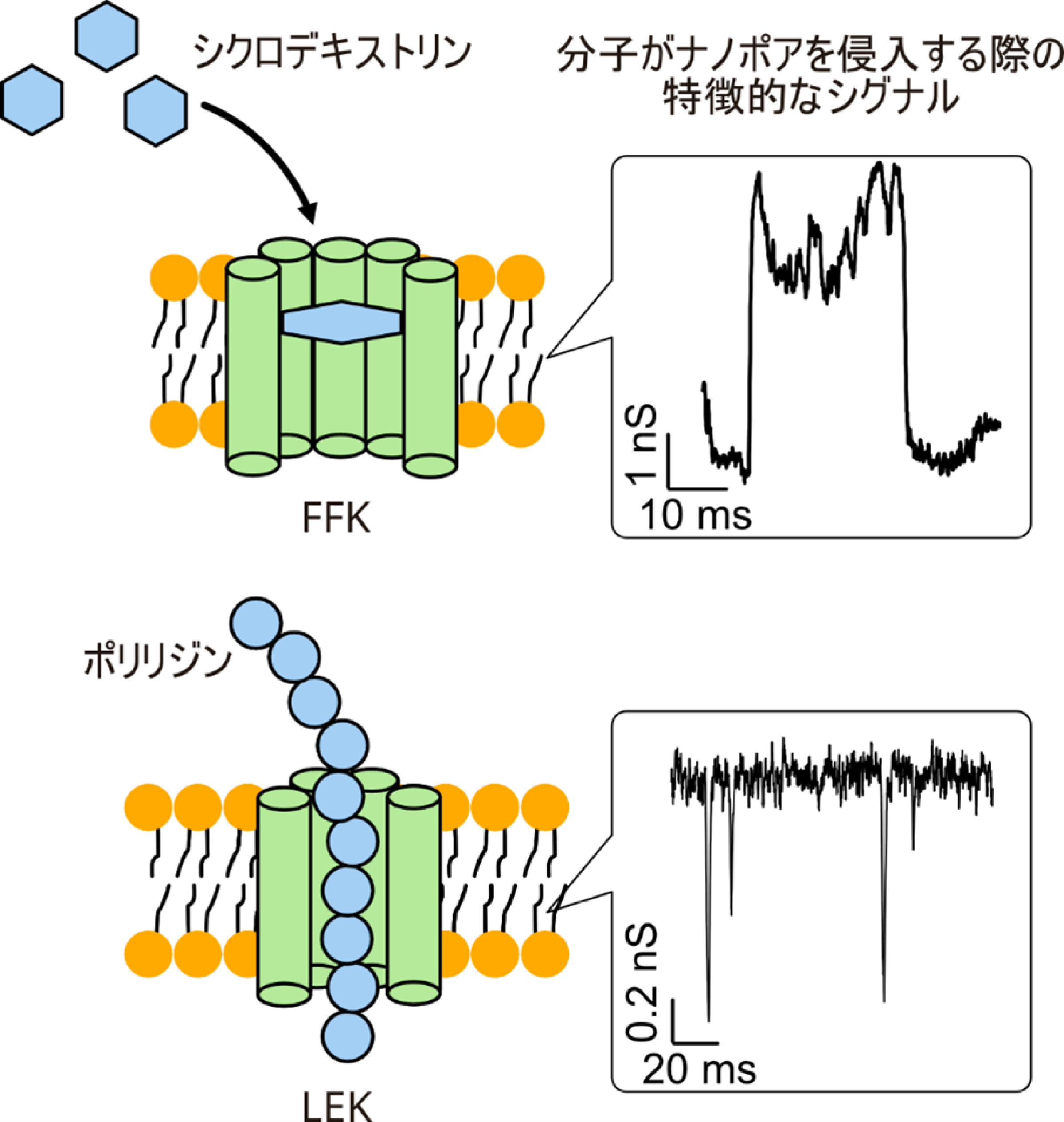
本研究では、天然タンパク質に多く見られる「GASモチーフ」と呼ばれる特徴的なアミノ酸の並び方に注目し、それを基にFFKとLEKという二種類の人工ペプチドを設計しました(図1)。シミュレーションと実験の結果、両者はいずれも人工細胞膜に孔を形成し、電流を通す機能を持つことが確認されました。さらに、FFKは複数の状態を行き来する動的な性質を示し、LEKは安定して孔を維持できるという特徴の違いが明らかになりました。加えて、糖の一種であるシクロデキストリンやアミノ酸の鎖であるポリリジンを用いた実験では、これらの分子がナノポアを侵入する際に電流変化が観測され、人工ナノポアによる“一分子検出”が実際に可能であることが示されました(図2)。
今後の展開
今回の成果は、人工的に設計したαヘリックス型のナノポアが一分子検出に成功した初めての例です。今後は、孔の大きさや形状をさらに精密に調整し、形成効率や安定性を高めることで、より多様な分子を識別できる高性能なナノポアを目指します。将来的には、DNAやタンパク質の高精度な解析に役立つバイオセンサーや、新しい医療診断ツール、さらには人工細胞や分子機械の部品として利用される可能性があります。
用語解説
[用語1]
ペプチド:2~50個程度のアミノ酸が短い鎖状につながった物質。
[用語2]
αヘリックス:アミノ酸が組み合わさって立体的な構造を作る際によく見られる、らせん型の構造。
[用語3]
ナノポア:膜タンパク質やイオンチャネルによって、脂質二分子膜中に形成されるナノメートル(1ミリメートルの100万分の1)サイズの微細な孔(ポア)。
[用語4]
GASモチーフ:グリシン(G)、アラニン(A)、セリン(S)などの小さなアミノ酸が並ぶことで、αヘリックス)同士が密に寄り添って安定した構造を作れるようにする配列。
論文情報
| 掲載誌 | ACS Nano |
|---|---|
| タイトル | De Novo Design of α-helical Peptide Nanopores for Single-molecule Detection using Helix Packing Motifs |
| 著者 | Zugui Peng, Masataka Usami, Ayaka Nakada, Yusuke Sekiya, Shoko Fujita, Batsaikhan Mijiddorj, Izuru Kawamura, Ryuji Kawano* |
| DOI | 10.1021/acsnano.5c15080 |
資料
研究者プロフィール
川村 出![]()
大学院工学研究院 教授
お問い合わせ先
<研究に関すること>
東京農工大学大学院工学研究院 生命機能科学部門 教授 川野 竜司
メールアドレス: プレスリリース記事内の連絡先を参照ください
<報道に関すること>
横浜国立大学総務企画部リレーション推進課
メールアドレス: press ynu.ac.jp
ynu.ac.jp
(担当:リレーション推進課)





